Przewlekła obturacyjna choroba płuc (POChP) to postępująca choroba o heterogennym charakterze, objawiającym się m. in. różnorodnym tempem utraty funkcji płuc 1. Najważniejszym zdarzeniem w historii naturalnej POChP są zaostrzenia, które stanowią katalizator progresji choroby i istotny czynnik zwiększający ryzyko incydentów sercowo-naczyniowych i zgonu 2,3. Nawet jedno umiarkowane zaostrzenie POChP związane jest z 2,5-krotnym wzrostem ryzyka ostrego zawału serca, udaru lub zgonu z przyczyn sercowo-naczyniowych* 3.
Dla optymalizacji leczenia POChP kluczowe jest oszacowanie ryzyka wystąpienia umiarkowanego lub ciężkiego zaostrzenia i możliwie jak najwcześniejsze dostosowanie terapii, w tym leczenia farmakologicznego, tak by zmniejszyć ryzyko wystąpienia zaostrzeń 4. Idealną sytuacją byłaby odpowiednia redukcja ryzyka jeszcze przed pierwszym umiarkowanym zaostrzeniem POChP – na wzór pierwotnej prewencji choroby wieńcowej 5. Jednakże, najbardziej skuteczne grupy leków, w tym terapię trójskładnikową wGKS/LAMA/LAMA, dotychczas stosowano często dopiero po wystąpieniu zaostrzenia POChP. Czy obecne dowody naukowe uzasadniają wcześniejszą eskalację farmakoterapii?
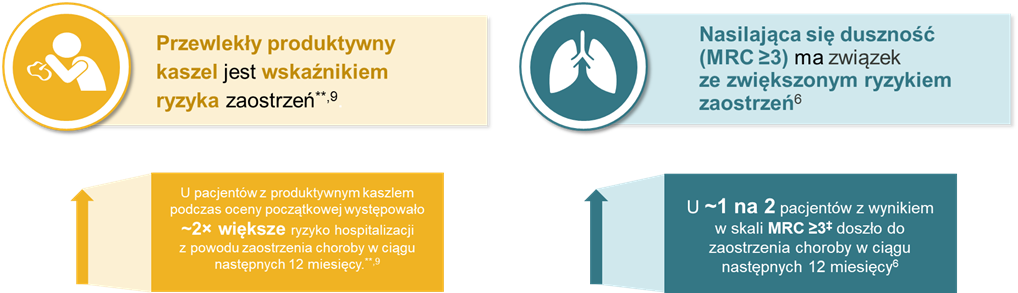
Mimo że najważniejszym predyktorem zaostrzeń POChP jest historia wcześniejszych zaostrzeń, to także pacjenci, którzy nie przebyli zaostrzenia, są na nie narażeni 6. Istnieje szereg innych, ważnych czynników ryzyka zaostrzeń POChP, m. in. nasilenie objawów, stopień obturacji i duszność 6-8.
Coraz częściej zwraca się uwagę również na przewlekły produktywny kaszel. Ten objaw zwiększa ryzyko wystąpienia zaostrzenia o 71%, a ryzyko hospitalizacji z powodu zaostrzenia prawie 2-krotnie** 9. Co więcej, kaszel ten wiąże się z 39% wyższym ryzykiem wystąpienia poważnego zdarzenia sercowo-naczyniowego lub oddechowego*** 10.,
Badanie KRONOS oceniało skuteczność i bezpieczeństwo połączenia budezonidu, glikopironium i formoterolu (BUD/GLY/FORM) u chorych na POChP z różną historią zaostrzeń i wysokim nasileniem objawów. Co ważne, 74% pacjentów nie miało historii zaostrzeń w ciągu ostatniego roku. Ponadto, pacjenci włączeni do badania KRONOS mieli duże nasilenie objawów (średni wynik CAT 18,0-18,7), pomimo wcześniejszego stosowania przynajmniej terapii dwuskładnikowej. Wykazano istotną redukcję częstości umiarkowanych lub ciężkich zaostrzeń o 52% u pacjentów przyjmujących BUD/GLY/FORM w porównaniu do ramienia LAMA/LABA† 11. W analizie post hoc badania KRONOS, uzyskano zbieżne wyniki dla pacjentów wyłącznie bez historii zaostrzeń w ciągu ostatniego roku. W takiej populacji uzyskano 48% redukcję częstości umiarkowanych lub ciężkich zaostrzeń vs LAMA/LABA†† 12.
Powyższe wyniki pokazują zasadność stosowania terapii trójskładnikowej w populacji pacjentów bez historii zaostrzeń, u których nie uzyskano odpowiedniej kontroli choroby pomimo stosowania terapii dwuskładnikowej. Co istotne, nieodpowiednia kontrola POChP może przybierać postać nasilonych objawów choroby, będących ważnym czynnikiem ryzyka zaostrzeń.
Na kongresie ATS 2024 zaprezentowano wyniki analizy post hoc badania KRONOS, oceniającej znaczenie przewlekłego produktywnego kaszlu dla efektywności BUD/GLY/FORM. Pierwszym wynikiem analizy było pokazanie, że u pacjentów bez historii zaostrzeń w ciągu ostatniego roku, niezależnie od grupy badania, przewlekły produktywny kaszel wiązał się z przynajmniej 1,9 razy wyższym ryzykiem wystąpienia umiarkowanego lub ciężkiego zaostrzenia POChP†††. W populacji pacjentów z przewlekłym produktywnym kaszlem i bez historii zaostrzeń, kombinacja BUD/GLY/FORM wykazała 41% redukcję ryzyka umiarkowanych lub ciężkich zaostrzeń w porównaniu do LAMA/LABA‡ 13.

Wysokie nasilenie objawów u pacjentów z POChP to ważny czynnik ryzyka zaostrzeń, który może rozpoczynać całą spiralę przyspieszonej progresji choroby. Pojawiające się dowody naukowe pokazują możliwość spowolnienia tej trajektorii. Nowe dane uzasadniają rozważenie eskalacji farmakoterapii do BUD/GLY/FORM u pacjentów bez historii zaostrzeń, którzy są jednak narażeni na ich wystąpienie poprzez wysokie nasilenie objawów, pomimo stosowania terapii dwuskładnikowej.
*Badanie rejestrowe obejmujące 118 807 przypadków MACE po zaostrzeniu POChP. MACE zdefiniowano jako ostry zawał serca, udar lub zgon z przyczyn sercowo-naczyniowych. Ryzyko wystąpienia MACE po zaostrzeniu wymagającym zastosowania doustnych glikokortykosteroidów: OR 2,50 (95% CI 2,40-2,61).
**Ryzyko wystąpienia zaostrzenia: OR 1,71 (95% CI 1,52-1,93). Ryzyko hospitalizacji z powodu zaostrzenia: OR 1,93 (95% CI: 1,50-2,48). Pacjenci z POChP i/lub astmą, n=5710. Przewlekły, produktywny kaszel zdefiniowano jako kaszel lub wytwarzanie plwociny występujące przez kilka lub większość dni w tygodniu w okresie ostatnich 3 miesięcy.
*** W ciągu 3 lat obserwacji. Ryzyko MACRE: skorygowany HR 1,39 (95% CI 1,11-1,74). Analiza danych pacjentów z POChP w badaniu NOVELTY (n=2295). Przewlekły, produktywny kaszel zdefiniowano jako kaszel lub wytwarzanie plwociny występujące przez kilka lub większość dni w tygodniu w okresie ostatnich 3 miesięcy. MACRE: nowa diagnoza ostrego zawału serca, niewydolności serca, choroby niedokrwiennej serca, zgon spowodowany chorobą układu sercowo-naczyniowego lub hospitalizacja zaostrzenia POChP.
†Badanie kliniczne III fazy pacjentów z umiarkowaną do bardzo ciężkiej POChP. Roczny wskaźnik występowania umiarkowanych lub ciężkich zaostrzeń: 0,46 (n=639) dla BUD/GLY/FORM i 0,95 (n=625) dla GLY/FORM. RR 0,48 (95% CI 0,37-0,64; p < 0,0001).
††Roczny wskaźnik występowania umiarkowanych lub ciężkich zaostrzeń: 0,41 (n=469) dla BUD/GLY/FORM i 0,80 (n=473) dla GLY/FORM. RR 0,52 (95% CI 0,37-0,72; niekorygowane p = 0,0001).
†††Populacja mITT. Częstość występowania zaostrzeń w zależności od statusu przewlekłego produktywnego kaszlu: grupa BUD/GLY/FORM: 0,47 (n=333) vs 0,15 (n=136); LAMA/LABA: 0,79 (n=320) vs 0,42 (n=153); wGKS/LABA: 0,45 (n=162) vs 0,19 (n=73); wGKS/LABA DPI open label: 0,67 (n=150) vs 0,07 (n=84). Przewlekły produktywny kaszel: punktacja ≥2 zarówno dla kaszlu, jak i dla obecności plwociny w teście CAT.
‡Populacja mITT. IRR 0,59 (95% CI: 0,40-0,87; nieskorygowane p=0,0078). IRR skorygowany dla odsetka przewidzianej FEV1 w punkcie wyjściowym (po podaniu leku rozszerzającego oskrzela) i liczby eozynofili we krwi w punkcie wyjściowym, jako zmiennych ciągłych oraz dla statusu korzystania z wGKS w okresie screeningu i kraju jako zmiennych kategorycznych. Przewlekły produktywny kaszel: punktacja ≥2 zarówno dla kaszlu, jak i dla obecności plwociny w teście CAT.
BID, dwa razy na dobę
BUD, budezonid
CAT, ang. COPD assessment test, test oceny POChP
CI, przedział ufności
DPI, inhalator suchego proszku
FEV1, natężona objętość wydechowa pierwszosekundowa
FORM, formoterol
GLY, glikopironium
HR, hazard względny
IRR, iloraz współczynników zapadalności
LABA, długo działający β2-agonista
LAMA, długo działający antagonista receptora muskarynowego
MACE, ang. major adverse cardiac event, poważne zdarzenie sercowo-naczyniowe
MRC, skala oceny nasilenia duszności według Medical Research Council
OR, iloraz szans
pMDI, inhalator ciśnieniowy z dozownikiem
POChP, przewlekła obturacyjna choroba płuc
RR, współczynnik częstości
wGKS, wziewny glikokortykosteroid
1. Welte T i wsp. Int J Clin Pract. 2015;69(3):336-349.
2. Suissa S i wsp. Thorax. 2012;67:957-963.
3. Reilev M i wsp. Respirology. 2019;24(12):1183-1190
4. GOLD. Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease: 2025 Report. https://goldcopd.org/2025-gold-report/ (data dostępu 07.2025).
5. Gupta R, Wood DA. Lancet. 2019;394(10199):685-696.
6. Müllerová H i wsp. BMJ Open 2014;4:e006171.
7. Hurst JR i wsp. N Engl J Med. 2010;363:1128-1138.
8. Lindberg A i wsp. Respir Med. 2015;109:88–95.
9. Hughes R i wsp. Respir Med. 2022;200:106921.
10. Rapsomaniki E i wsp. Poster PA1928 zaprezentowany na ERS 2023, Mediolan, Włochy, 09-13.09.2023. https://bit.ly/3qk5A6v (data dostępu 23.02.2024).
11. Ferguson GT i wsp. Lancet Respir Med. 2018;6(10):747-758.
12. Martinez FJ i wsp. Int J Chron Obstruct Pulmon Dis 2021;16:179–189.
13. Marshall J i wsp. Am J Respir Crit Care Med 2024;209:A1850.
14. Aktualna Charakterystyka Produktu Leczniczego Trixeo Aerosphere.