Astma eozynofilowa to często występujący rodzaj astmy charakteryzujący się podwyższoną liczbą eozynofilów, które mogą powodować
zapalenie dróg oddechowych.1-3
U maksymalnie 10% osób
z astmą występuje ciężka astma4
Do 70% pacjentów
z ciężką astmą cierpi na astmę eozynofilową*5
*Większość pacjentów z ciężką astmą (stopnia 3. = najprawdopodobniej eozynofilową) miała liczbę eozynofili we krwi (BEC) na poziomie ≥300 komórek/µl LUB była w trakcie leczenia anty-IL-5/IL-5R. Ciężka choroba została również scharakteryzowana jako BEC na poziomie ≥150–300 komórek/μl i konieczność przyjmowania doustnych kortykosteroidów (OCS) w terapii podtrzymującej lub obecność ≥2 polipów nosa (NP), podwyższony poziom cząstkowego tlenku azotu (FeNO) i późny początek choroby.
Rola immunologicznej dysfunkcji eozynofilów w astmie eozynofilowej
Eozynofile to kluczowe komórki efektorowe w astmie eozynofilowej, w przypadku której zaburzenia czynności układu odpornościowego prowadzą do zapalenia eozynofilowego w tkance dróg oddechowych.6-8
Zwiększenie liczby eozynofilów w drogach oddechowych wiąże się ze wzrostem nasilenia astmy.9
Pacjenci z astmą eozynofilową są narażeni na częstsze zaostrzenia, słabszą kontrolę astmy i obniżoną czynność płuc.10-12
Zapalenie eozynofilowe w tkance dróg oddechowych7,13-16
W przypadku astmy eozynofilowej komórki odpornościowe aktywowane przez czynniki alergiczne i niealergiczne mogą wydzielać różne cytokiny. Cytokiny wytwarzane przez te komórki mogą przyczynić się do rekrutacji, aktywacji i przeżycia eozynofili.11,16-18
Cytokiny to białka sygnalizujące, które zwykle mają rozmiar mniejszy niż 80 kDa. Poprzez przekazywanie sygnałów pozakomórkowych białka te regulują szeroki zakres funkcji, w tym odporność wrodzoną i nabytą, hematopoezę, stan zapalny i proces naprawy oraz proliferację.19
Eozynofile są kluczowymi komórkami efektorowymi i mogą być przyczyną ciężkiej astmy u pacjentów.6-8
Jak rozpoznać astmę eozynofilową?
U pacjentów z astmą eozynofilową mogą wystąpić następujące cechy kliniczne11,20:
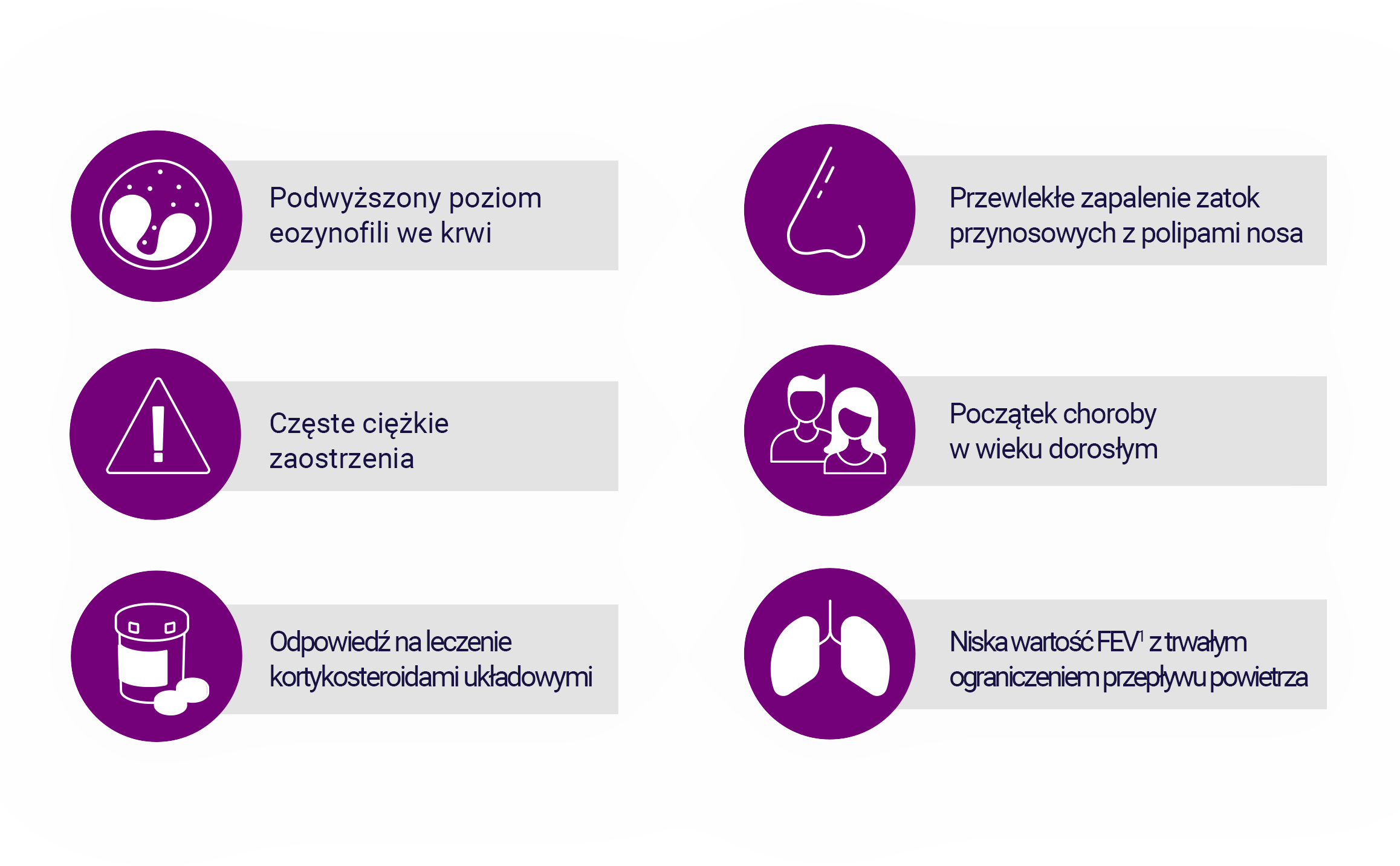
Ważne jest, aby wykluczyć eozynofile jako czynnik wywołujący ciężką chorobę u pacjentów z astmą.
Bibliografia:
1. Wenzel S. Severe asthma in adults. Am J Respir Crit Care Med. 2005;172:149-160.
2. Coumou H, Bel EH. Improving the diagnosis of eosinophilic asthma. Expert Rev Respir Med. 2016;10(10):1093-1103.
3. Trivedi SG, Lloyd CM. Eosinophils in the pathogenesis of allergic airway disease. Cell Mol Life Sci. 2007;64(10):1269-1289.
4. Chung KF, Wenzel SE, Brozek JL, et al. International ERS/ATS guidelines on definition, evaluation and treatment of severe asthma. Eur Respir J. 2014;43(2):343-373.
5. Perez-de-Llano L, Tran TN, Al-ahmad M, et al. Characterization of eosionophilic and non-eosinophilic severe asthma phenotypes and proportion of patients with these phenotypes in the International Severe Asthma Registry (ISAR). Am J Respir Crit Care Med. 202; 201: A4525.
6. Rothenberg ME, Hogan SP. The eosinophil. Ann Rev Immunol. 2006;24:147-174.
7. Robinson D, Humbert M, Buhl R, et al. Revisiting Type 2-high and Type 2-low airway inflammation in asthma: current knowledge and therapeutic implications. Clin Exp Allergy. 2017;47(2):161 175.
8. George L. Brightling CE Eosinophilic airway inflammation: role in asthma and chronic obstructive pulmonary disease. Ther Adv Chronic Dis. 2016;7(1):34-51.
9. Bousquet J, Chanez P, Lacoste JY, et al. Eosinophilic inflammation in asthma. N Engl J Med. 1990;323(15):1033-1039.
10. Price DB, Rigazio A, Campbell JK, et al. Blood eosinophil count and prospective annual asthma disease burden: a UK cohort study. Lancet Respir Med. 2015;3:849-858.
11. de Groot JC, ten Brinke A, Bel EH. Management of the patient with eosinophilic asthma: a new era begins. ERJ Open Res. 2015;(1):00024-2015.
12. Newby C, Agbetile J, Hargadon B, et al Lung function decline and variable airway inflammatory pattern: longitudinal analysis of severe asthma. J Allergy Clin Immunol. 2014;134:287-294.
13. Mukherjee M, Sehmi R, Nair P. Anti-IL5 therapy for asthma and beyond. World Allergy Organ J. 2014;7(1):32.
14. Lambrecht BN, Hammad H. The immunology of asthma. Nat Immunol. 2015;16(1)45-56.
15. Gandhi NA, Bennett BL, Graham NMH, et al. Targeting key proximal drivers of type 2 inflammation in disease. Nat Rev Drug Discov. 2016;15(1):35-50.
16. McBrien CN, Menzies-Gow A. The biology of eosinophils and their role in asthma Front Med (Lausanne). 2017;4:93.
17. Fulkerson PC, Rothenberg ME. Targeting eosinophils in allergy, inflammation, and beyond. Nat Rev Drug Discov. 2013:12(2);117-129.
18. Hogan SP, Rosenberg HF, Moqbel R, et al. Eosinophils: biological properties and role in health and disease. Clin Exp Allergy. 2008:38(5);709-750.
19. Chung KF. Cytokines. In:Barnes PF, Drazen JM, Rennard SI, Thomson NC, eds. Asthma and COPD: Basic Mechanisms and Clinical Management, 2nd ed. Academic Press; 2009:327-341.
20. de Groot JC, Storm H. Amelink M, et al. Clinical profile of patients with adult-onset eosinophilic asthma. ERJ Open Res. 2O16;2(2):00100-2015.
Informacje zawarte na tej stronie internetowej są dostarczane przez firmę AstraZeneca wyłącznie w celach edukacyjnych i są przeznaczone wyłącznie dla pracowników służby zdrowia.
