Terapia ciężkiej astmy mimo pojawiających się nowych możliwości terapeutycznych nadal stanowi jedno z największych wyzwań współczesnej pulmonologii i alergologii. Doustna sterydoterapia jest w wielu przypadkach skuteczna, ale niesie ze sobą ryzyko wielu działań niepożądanych. Nowe leki biologiczne w sposób bardziej spersonalizowany leczą pacjentów z określonym fenotypem i endotypem choroby. Jednym z najczęściej występujących fenotypów ciężkiej astmy jest fenotyp eozynofilowy. Leki biologiczne rekomendowane w tym fenotypie to przeciwciała skierowane przeciwko IL5 (mepolizumab, reslizumab) oraz receptorowi dla IL5 (benralizumab)1 2. Powodują one redukcję liczby eozynofilów w surowicy krwi, a co bardziej istotne- w miejscu toczącego się procesu zapalnego3. W przypadku terapii benralizumabem mamy do czynienia z niemal całkowitą deplecją eozynofilów w surowicy krwi już w 1. dobie od podania leku4. Poniższy artykuł podsumowuje profil bezpieczeństwa leków anty-eozynofilowych na przykładzie benralizumabu u chorych na ciężką astmę.
Rola eozynofilów w procesie zapalnym.
Rozwój i dojrzewanie eozynofilów odbywa się w szpiku kostnym pod wpływem IL-5, IL-3 i GM-CSF5. IL-5 odpowiada m.in. za końcowy etap dojrzewania eozynofilów i ich migrację do krwi krążącej, receptor CCR3 odgrywa natomiast kluczową rolę w promowaniu rekrutacji eozynofilów do narządów i tkanek6.
Eozynofile odgrywają istotną rolę w procesach zapalnych w różnych tkankach i narządach7 prowadząc ostatecznie do uszkodzenia i przebudowy tkanek8
Więcej informacji na temat patofizjologii eozynofila znajdziesz tutaj
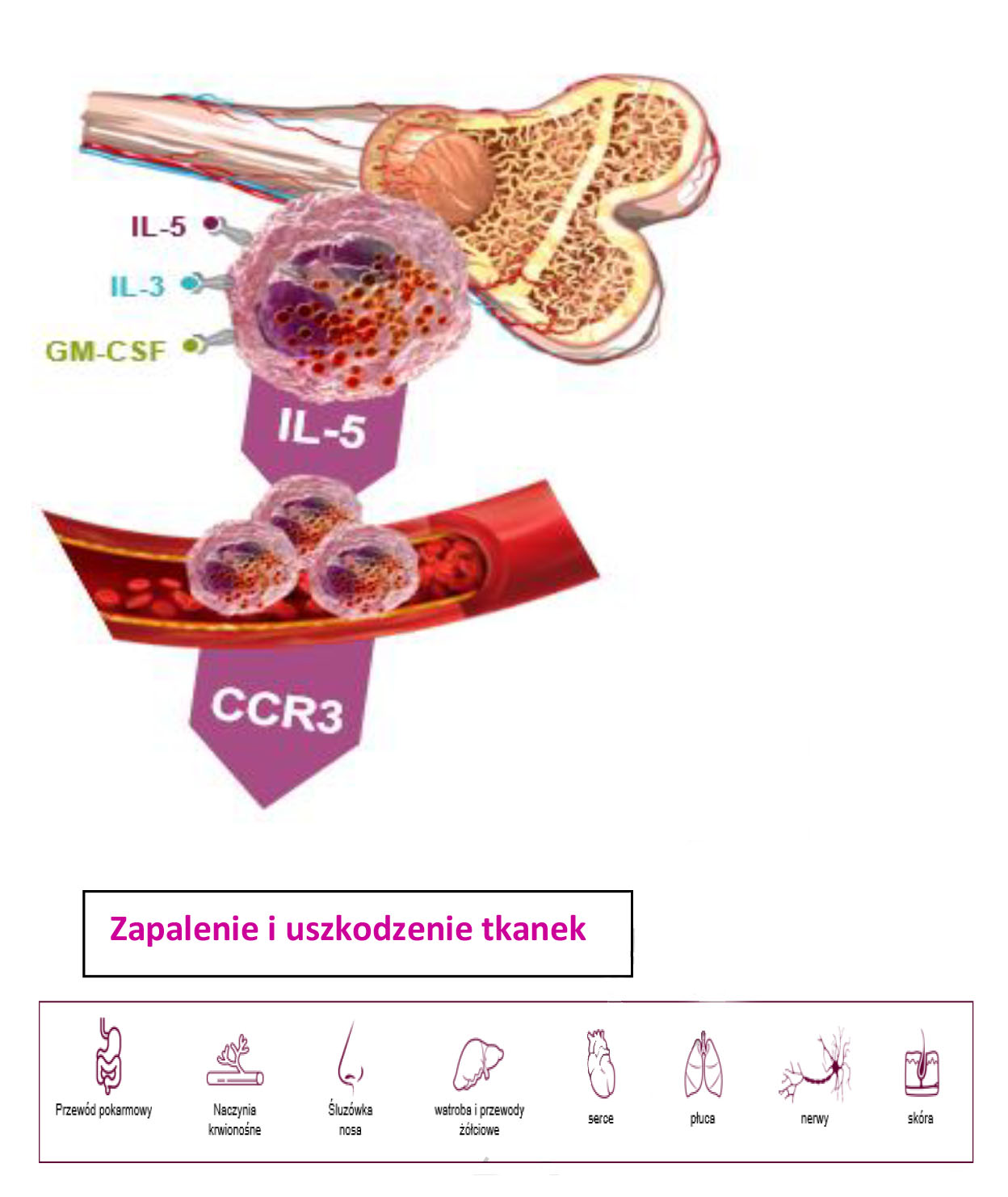
Etapy rozwoju eozynofilów i ich rola w procesie zapalnym.
Brak eozynofilów u ludzi nie wywołuje żadnych nieprawidłowości.
Pacjenci pozbawieni eozynofilów nie wykazują żadnych nieprawidłowości w przeciwieństwie do np. pacjentów z niedoborami czynników odporności i chorobami alergicznymi.9
Dane z badań nad profilem bezpieczeństwa terapii przeciwciałami monoklonalnymi anty- IL-5 skierowanymi bezpośrednio (benralizumab przez receptor IL-5) lub pośrednio (mepolizumab i reslizumab przez IL-5) przeciwko eozynofilom, w efekcie których dochodzi do prawie całkowitej lub częściowej deplecji eozynofilów, potwierdzają , że są one dobrze tolerowane10 11 12
Stanowisko prezesa PTA prof. dr hab. n. med. Macieja Kupczyka dotyczące bezpieczeństwa całkowitej deplecji eozynofilów dostępne pod linkiem.
Profil bezpieczeństwa benralizumabu jest zbliżony do placebo.
Badania fazy 2. oceniające skuteczność i bezpieczeństwo benralizumabu w astmie oskrzelowej rozpoczęły się w 2010 (n= 964), natomiast fazy 3. w 2013 r. (n= 2892)13 W badaniach 3.fazy profil bezpieczeństwa benralizumabu nie różni się istotnie od profilu placebo.14 Przedłużone badanie oceniające bezpieczeństwa benralizumabu (BORA) w obserwacji 2-letniej również nie dostarczyło żadnych nowych sygnałów alarmujących o zwiększonym ryzyku związanym z
deplecją eozynofilów15 Więcej informacji o badaniu BORA znajdziesz tutaj.
Benralizumab był ogólnie dobrze tolerowany przez pacjentów, bez wyraźnego związku między leczeniem a zwiększonym ryzykiem zakażeń lub nowotworów złośliwych16. Nie odnotowano również w badaniach klinicznych z udziałem benralizumabu ani jednego przypadku infestacji pasożytniczej, mimo, że rekrutacja pacjentów odbywała się również w regionach endemicznych17 18
Ostatnio opublikowane dane na podstawie badania MELTEMI obejmującego długotrwałą obserwację chorych leczonych benralizumabem (do 5 lat) potwierdziły, że profil bezpieczeństwa benralizumabu jest zbliżony do placebo. Podobnie jak w badaniach 3. fazy nie zaobserwowano zwiększonego ryzyka występowania nowotworów ani innych sygnałów ostrzegawczych związanych z deplecją eozynofilów19
Więcej informacji na temat badania MELTEMI znajdziesz tutaj. Wyniki badania wraz z komentarzem eksperta są zaprezentowane w poniższym wideo.
1. Tan LD, Bratt JM, Godor D, et al. J Asthma Allergy. 2016;9:71–81. doi:10.2147/JAA. S78049. eCollection 2016.
2. Bel EH, ten Brinke A. New Anti-Eosinophil Drugs for Asthma and COPD: Targeting the Trait CHEST 2017;152 (6): 1276-1282.
3. Leckie M., ten Brinke A., Khan J., Diamant Z., O’Connor B., Walls C., et al. (2000) Effects of an interleukin-5 blocking monoclonal antibody on eosinophils, airway hyper-responsiveness, and the late asthmatic response. Lancet 356: 2144–2148.
4. Charakterystyka Produktu Leczniczego Benralizumab.
5. Ramirez GA, Yacoub M-R, Ripa M, et al. Eosinophils from physiology to disease: a comprehensive review. BioMed Res Int. 2018;2018:9095275.
6. Ramirez GA, Yacoub M-R, Ripa M, et al. Eosinophils from physiology to disease: a comprehensive review. BioMed Res Int. 2018;2018:9095275.
7. Ramirez GA, Yacoub M-R, Ripa M, et al. Eosinophils from physiology to disease: a comprehensive review. BioMed Res Int. 2018;2018:9095275
8. Ackerman SJ BloodJ 2012;Volume 122 Number 5
9. Gleich GJ, Klion AD, Lee JJ, et al. The consequences of not having eosinophils. Allergy. 2013;68 829-835.
10. Charakterystyka Produktu Leczniczego Benralizumab
11. Charakterystyka Produktu Leczniczego Mepolizumab
12. Charakterystyka Produktu Leczniczego Reslizumab
13. ClinicalTrial.gov [Internet]. National Library of Medicine (US)
14. Charakterystyka Produktu Leczniczego Benralizumab
15. Busse WW, et al. Long-term of benralizumab in patients with severe, uncontrolled asthma: 1-year results from the BORA phase 3 extension trial. Lancet Respir Med. 2019;7:46-59
16. David J. Jackson Safety of Eosinophil-Depleting Therapy for Severe, Eosinophilic Asthma: Focus on Benralizumab Drug Saf 2020 May;43(5):409-425. doi: 10.1007/s40264-020-00926-3.
17. Charakterystyka Produktu Leczniczego Benralizumab
18. Busse WW, et al. Long-term of benralizumab in patients with severe, uncontrolled asthma: 1-year results from the BORA phase 3 extension trial. Lancet Respir Med 2019 Jan;7(1):46-59. doi: 10.1016/S2213-2600(18)30406-5
19. Korn S, i wsp. The Journal of Allergy and Clinical Immunology: In Practice (2021), doi: https://doi.org/10.1016/ j.jaip.2021.07.05